Notícias
- Material Didático
- Materiais - FundamentosEmpacotamento Atômico dos Cristais - Introdução
Por causa da natureza da ligação metálica, os átomos de um metal podem ser visualizados como esferas rígidas. As forças entre eles são portanto isotrópicas.
Os átomos são organizados em um arranjo(reticulado) espacial, que é uma coleção tridimensional de pontos, onde cada ponto do arranjo (reticulado) é idêntico a qualquer outro ponto. O reticulado pode ser descrito pela célula unitária (modelo geométrico), que é a menor unidade de repetição do reticulado.
Em alguns metais, como por exemplo o Al e o Mg, é mais simples visualizar os átomos como um empilhamento de camadas, onde cada átomo tem 12 vizinhos (outros átomos) mais próximos, 6 em seu próprio plano, 3 no plano superior adjacente e 3 no plano inferior. Estas são as chamadas estruturas compactas.
A característica mais óbvia da estrutura cristalina é que ela é regular e repetitiva. A célula unitária permite descrever qualquer tipo estrutura como um todo, porque a estrutura completa pode ser gerada pela repetição da célula unitária no espaço. Há apenas sete formas de célula unitária que podem ser empilhadas para formar os sistemas cristalinos no espaço tridimensional. Elas são:
| cúbica | tetragonal | ortorrômbica | romboédrica |
| hexagonal | monoclínica | triclínica |
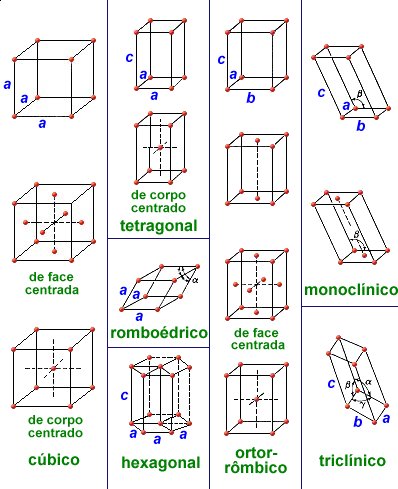
Destes sistemas cristalinos podemos identificar 14 tipos diferentes de células unitárias, conhecidas como Redes de Bravais. Cada uma destas células unitárias tem certas características que ajudam a diferenciá-las das outras células unitárias. Além do mais, estas características também auxiliam na definição das propriedades de um material particular.
Gostou? Então compartilhe:
Notícias relacionadas
