Notícias
Água doce inclui todas as águas naturais não salinas, poluídas ou não, encontradas em córregos, rios, lagos e lagoas. Nesta categoria também são incluídas águas oriundas de precipitações como chuva e neve, água de poços, nascentes e águas tratadas.
A durabilidade dos aços em contato com este tipo de água depende das seguintes características:
Efeito de gases dissolvidos
De todas as características da água que influenciam a taxa de corrosão, os gases dissolvidos é provavelmente a mais importante.
Oxigênio: a taxa com que o oxigênio atinge a superfície de um metal controla a taxa de corrosão e pode determinar se ocorre corrosão aeróbica ou anaeróbica. O oxigênio também acelera as ações do dióxido de carbono, do sulfeto de hidrogênio e de outros gases e sólidos.
O dióxido de carbono tem uma ação corrosiva em torno de um décimo da do oxigênio. Em águas doces a concentração de dióxido de carbono é importante pela sua influência na solubilidade e precipitação do carbonato de cálcio.
O sulfeto de hidrogênio pode causar ataque muito rápido no aço, mesmo na ausência de oxigênio. Os produtos da corrosão anaeróbica são enxofre e sulfeto de ferro, ambos catódicos em relação ao ferro, que tendem a causar corrosão localizada (pitting). A maioria dos problemas de corrosão devidos ao sulfeto de hidrogênio ocorre quando este gás é produzido por bactérias.
Efeito do pH
Existe pouca diferença na taxa de corrosão de aços em água doce com valores de pH entre 4,5 e 9,5. Isto pode ser confirmado para águas “de torneira” e água destiladas. Neste campo de valores de pH , os produtos da corrosão mantém um pH de 9,5 em ponto próximos da superfície do aço, independentemente do pH da solução . Para valores de pH em torno de 4 e abaixo começa a evolução do hidrogênio e a corrosão aumenta rapidamente (ver figura abaixo).
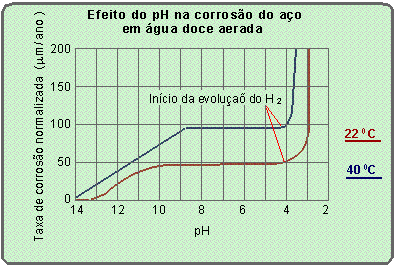
A maioria dos sais dissolvidos em água tende a reduzir tanto a solubilidade do oxigênio como a do hidróxido de ferro. Então, as taxas de corrosão em soluções concentradas de sal são usualmente menores do que em soluções diluídas de sal. Alguns sais, também tendem a elevar o pH, o que reduz a tendência a corrosão ácida.
Por outro lado, a maioria dos sais dissolvidos se ioniza e aumenta a condutividade da água, que por sua vez tende a concentrar a corrosão levando a ataque severo (pitting). A condutividade aumentada faz crescer as áreas catódicas e favorece a combinação dos produtos das reações do catodo e do anodo com a água, no lugar da combinação na superfície de corrosão.
A corrosão é favorecida pelos cátions na seguinte ordem: magnésio, cádmio, manganês, cálcio, estrôncio, bário, lítio, sódio, potássio amônio, cromo trivalente e ferro trivalente.
Sais de amônia e sais de elementos trivalentes como cromo e ferro estimulam fortemente a corrosão porque se hidrolizam criando condições ácidas. A corrosão ocorre então por evolução do hidrogênio e também por despolarização do oxigênio. O Cloreto de amônia é particularmente ativo, mesmo em concentrações baixas como 10 ppm.
Íons de cobre e mercúrio: íons solúveis de cobre e mercúrio são capazes de reagir exotermicamente com o ferro do aço, substituindo-o. Os íons dissolvidos (que são mais nobres que o ferro) depositam-se na superfície do aço enquanto o mesmo número de átomos de ferro entra em solução. A substituição mútua pode correr na ausência de oxigênio e não existe inibidor capaz de impedir esta reação.
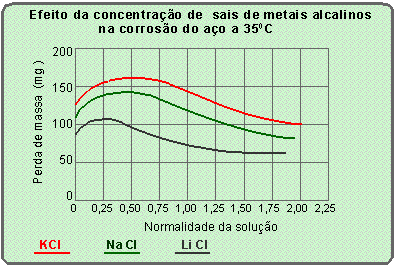
Sais de metais alcalinos: quando sais de lítio, sódio ou potássio são adicionados à água aerada, a taxa de corrosão varia com a concentração. Em pequenas concentrações, a adição de um sal de metal alcalino aumenta a taxa de corrosão. Em concentrações mais altas, a taxa de corrosão atinge o valor máximo e então decresce com o aumento posterior da concentração, como mostrado na figura abaixo.
Gostou? Então compartilhe:
Notícias relacionadas
Faça seu login
Ainda não é cadastrado?
Cadastre-se como Pessoa física ou Empresa
