Notícias
Um metal no estado sólido possui átomos que vibram com uma certa freqüência em torno de posições geométricas definidas (determinadas pelo tipo de arranjo cristalino específico do metal em questão).
No estado líquido, tais átomos, além de vibrarem, não possuem posição definida, pois estão em movimento dentro do líquido.
Por se movimentarem, os átomos no estado líquido entram em colisão, envolvendo milhares de átomos simultaneamente.
Pode-se imaginar que nesta colisão, surge um agrupamento momentâneo de átomos, formando um núcleo , com um dado arranjo atômico (CCC, CFC, HC, etc). O núcleo é um sólido que pode crescer ou se dissolver, dependendo da temperatura do sistema. O crescimento do sólido se dá por migração de átomos do liquido para o sólido, acoplando os átomos nas posições de equilíbrio do reticulado que é específico do metal em questão, conforme indicado na figura.
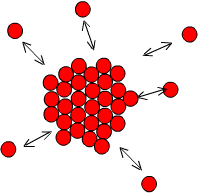
A temperatura na qual ocorre equilíbrio termodinâmico entre um sólido e seu respectivo líquido é a temperatura de fusão (que é igual à de solidificação apenas em substâncias puras e sistemas eutéticos). Contrariamente ao senso comum, tal definição não significa que a solidificação se inicia nesta temperatura.
O estudo da solidificação envolve duas abordagens distintas. Na abordagem termodinâmica, analisam-se as energias envolvidas na solidificação enquanto na abordagem cinética, analisa-se a velocidade com que os processos (de nucleação e crescimento) acontecem.
Trataremos aqui da abordagem termodinâmica
A solidificação é composta dos processos de NUCLEAÇÃO e CRESCIMENTO DE CRISTAIS a partir de um líquido. Ocorre no resfriamento, conforme curva de temperatura abaixo.
.gif)
CURVA TÍPICA DE TEMPERATURAS DE RESFRIAMENTO
Na região L (estado líquido) , a temperatura diminui por efeito de transmissão de calor através do molde. A temperatura aumenta a Partir de Tf -DT pelo efeito de rescalescência. Inicia-se a solidificação, através do aparecimento dos primeiros núcleos sólidos.No patamar L+S há a coexistência dos estados líquido e sólido. Ao final do patamar toda a massa está solidificada ( início da região S).
Note: a solidificação se inicia numa temperatura situada no intervalo DT, portanto o líquido se encontra abaixo da temperatura de fusão ( Tf ),super-resfriado.
Em sistemas sob pressão e temperatura constantes, a energia controladora do processo é a energia livre de Gibbs (G).
Tal energia é definida por
G = H -TS,
onde T é a temperatura, H é a entalpia e S a entropia da substância em questão.
A entalpia pode ser entendia fisicamente como uma medida da quantidade de calor existente na substância e a mesma é “estocada” na forma de amplitude de vibração dos átomos. Portanto, a medida da entalpia (unidades de energia) reflete uma medida da energia de ligação entre os átomos.
Por sua vez, a entropia pode ser entendida como uma medida da desorganização interna da substância, isto é, uma medida de como os átomos se arranjam. Em um líquido, os átomos se arranjam de modo desordenado enquanto em um sólido, há maior ordenação (menor entropia), pois os átomos ocupam posições regulares (formando o reticulado cristalino CCC, CFC e outros).
Sabe-se que no universo a energia é constante e que a variação da entropia é igual ou maior que zero (tendência à desordem)
A energia de Gibbs é portanto um parâmetro indicador da estabilidade em sistemas sob temperatura e pressão constantes. O sistema tende a seu estado de mínima energia livre.
Para o caso de transformação de fases numa substância, trabalha-se com a variação da energia livre DG , na forma:
DG= G sólido – G líquido ou DG = DH-TDS
onde DH é a variação de entalpia e DS é a variação de entropia entre os estados da transformação (líquido e sólido).
Como conseqüência do fato de que o sistema (sob temperatura e pressão constantes) tende a evoluir no sentido de minimizar a energia livre de Gibbs, temos que a variação desta energia (DG) é um valor que indica o sentido espontâneo de uma reação (quando o sistema se encontra sob temperatura e pressão constantes), de acordo com:
se DG > 0 : reação impossível (não ocorre)
se DG = 0 : reação em equilíbrio
se DG < 0 : reação pode ocorrer (sentido espontâneo)
Além do aspecto de que o valor de DG indica a tendência de reação , tal valor é uma medida da energia disponível para que ocorra a reação, podendo ser interpretado como a força motriz da transformação. Quanto mais negativo for DG, maior a força motriz e maior a tendência de ocorrer a reação.
O objeto deste enfoque é a energia envolvida no processo, particularmente a força motriz e a barreira energética.
A nucleação é um fenômeno que pode ocorrer com a formação de núcleos diretamente a partir do líquido (nucleação homogênea) ou com a formação de núcleos sobre superfícies pré-existentes (nucleação heterogênea), abordadas abaixo:
Nucleação Homogênea
O início da solidificação ocorre com a formação de núcleos sólidos estáveis que posteriormente crescem.
Para que haja formação destes núcleos, é preciso que DG£ 0 .
Por outro lado, a formação de um núcleo envolve duas energias.
A primeira é uma energia de volume (DGVOL), resultante da transformação do líquido em sólido e que é liberada pelo sistema, atuando como força motriz da solidificação.
A segunda é uma energia de superfície (DGSUP), pois o surgimento do núcleo implica na criação de uma interface entre sólido e líquido, que exige consumo de energia pelo sistema e atua como barreira à solidificação.
Assim,
DGTOTAL= DGSUP + DGVOL£ 0
Uma vez que a nucleação se inicia com um certo super-resfriamento, DGVOL é sempre negativo sendo a força motriz do processo de solidificação. Assumindo-se que o núcleo inicial seja esférico, tal variação de volume é proporcional ao cubo do raio da esfera. (DGVOL ~ R3 )
Por outro lado, a criação da interface sólido-líquido exige consumo de energia e o DGSUP é positivo e proporcional à superfície da esfera, isto é, proporcional ao quadrado do raio (DGSUP ~R2).
As energias são ilustradas na figura abaixo:
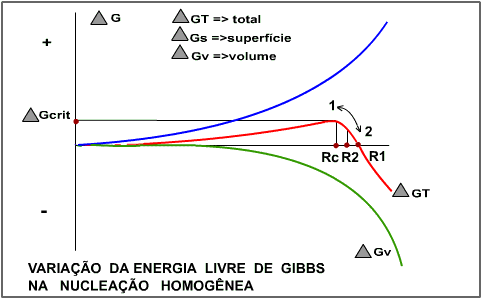
Observa-se que o DGTOTAL é menor que zero para raio do núcleo igual a R1, o que sugere que o menor núcleo estável é aquele que possui raio R1.
Todavia, caso se forme momentaneamente um núcleo com raio igual a R2, (onde D GTOTAL > 0), tem-se duas possibilidades:
O núcleo pode perder átomos para o líquido, reduzindo seu tamanho e, conseqüentemente, aumentando DGTOTAL (seta 1), o que é termodinamicamente impossível (aumentar DG significa DG>0)
Outra possibilidade é o núcleo receber átomos do líquido, aumentando seu tamanho e, conseqüentemente, diminuindo DGTOTAL (seta 2), o que é termodinamicamente viável (DG < 0).
Portanto, qualquer núcleo momentaneamente formado com tamanho entre Rc e R1, embora tenha gerado um DGTOTAL > 0 (o que o torna instável), tende a crescer (direção da seta 2) pois isto reduz o DGTOTAL.
Do exposto resulta que existe um tamanho mínimo para que os núcleos possam crescer e se tornar estáveis. Este tamanho mínimo recebe o nome de raio crítico (Rc).
A este reio crítico corresponde um DGCRIT , que é a barreira energética a ser vencida para haver solidificação. Esta barreira energética tem origem na necessidade de criar superfície (DGSUP, que consome energia) e por isso surge a necessidade de haver um certo super-resfriamento para que o líquido acumule energia volumétrica (DGVOL, força motriz) capaz de compensar tal barreira energética.
Nucleação heterogênea
A nucleação heterogênea ocorre quando a solidificação ocorre a partir de superfícies pré-existentes, tais como as paredes do molde ou quando da presença de partículas sólidas no líquido.
A figura abaixo ilustra que a superfície a ser criada pela nucleação a partir de um substrato (nucleação heterogênea) é menor, (comparada a da nucleação homogênea) podendo facilitar o processo pois exige menor energia de interface (barreira energética) .
Observa-se também que o núcleo resultante da presença de um substrato possui menor volume e portanto menor número de átomos.
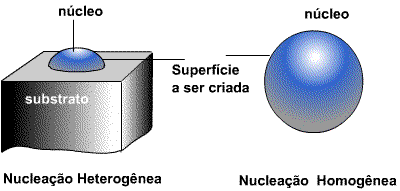
A presença de qualquer tipo substrato não é garantia de facilitar a nucleação, pois depende da tensão superficial entre núcleo e substrato, isto é, depende da molhabilidade entre ambos que, por sua vez, depende da composição química do núcleo e do substrato. Esta molhabilidade pode ser avaliada pelo ângulo
A análise termodinâmica realizada para a nucleação homogênea pode ser aplicada para a nucleação heterogênea, porém substituindo-se a variável raio pela variável número de átomos (N) que constituem um núcleo.
Caso haja molhabilidade entre líquido e substrato, a energia crítica para nucleação torna-se menor, conforme ilustrado abaixo (quanto maior a molhabilidade, menor é o ângulo q e menor DGcrit para nucleação heterogênea).
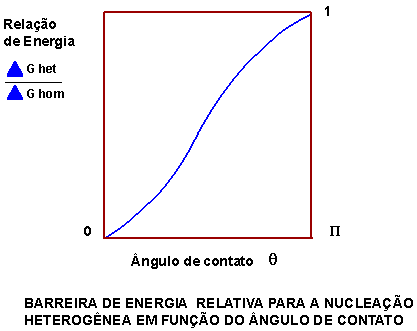
A figura abaixo ilustra as parcelas de energia de superfície, volumétrica e total para o caso de nucleação com e sem substrato (índices 2 e 1 respectivamente).
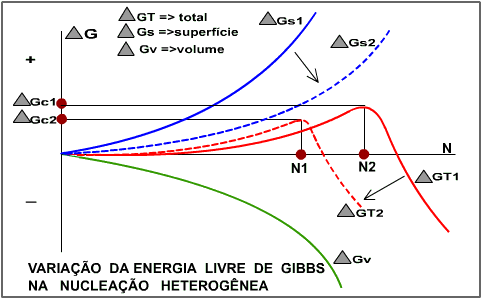
A presença de um substrato diminui (de DGS1 para DGS2) a energia de interface a ser criada (pois parte desta já existe no substrato), reduzindo a energia crítica total (de DGC1 para DGC2) e portanto o número de átomos necessários para formar o núcleo crítico (de N1 para N2), facilitando a nucleação. (A presença de substrato diminui o número de átomos, mas não diminui o raio crítico).
Gostou? Então compartilhe:
Notícias relacionadas
Faça seu login
Ainda não é cadastrado?
Cadastre-se como Pessoa física ou Empresa
